Cara Memahami Tabel Periodik Kimia Melalui Logika Sains
Pernahkah Anda merasa pusing saat menatap lembaran penuh kotak dan simbol unsur di dinding laboratorium sekolah? Banyak siswa beranggapan bahwa satu-satunya cara menguasai materi ini adalah dengan menghafal seluruh isi tabel tersebut. Padahal, cara memahami tabel periodik kimia yang paling efektif bukanlah melalui ingatan jangka pendek, melainkan dengan mengenali pola perilaku unsur di alam semesta.
Baca Juga: Mengenal Sekolah Terpopuler di Jambi Inilah Pilihan Favorit
Dmitri Mendeleev tidak menyusun tabel ini secara acak. Beliau melihat adanya keteraturan sifat yang berulang. Jika Anda memahami “bahasa” di balik posisi sebuah unsur, Anda bisa memprediksi sifat kimia tanpa perlu melihat buku teks sama sekali. Mari kita mulai petualangan logika ini dengan melihat bagaimana atom berinteraksi di dunia nyata.
Membedah Golongan Melalui Eksperimen Logam Alkali
Salah satu cara paling menarik untuk melihat keteraturan tabel periodik adalah melalui pengamatan logam alkali di Golongan 1. Jika Anda melihat demonstrasi memasukkan sedikit logam Natrium (Na) ke dalam air, akan terjadi ledakan kecil yang energetik. Namun, coba bandingkan dengan Kalium (K) yang berada tepat di bawahnya; reaksinya jauh lebih dahsyat.
Mengapa hal ini terjadi? Jawabannya terletak pada struktur atomnya. Semakin ke bawah posisi unsur dalam satu golongan, jari-jari atomnya semakin besar. Elektron terluar menjadi semakin jauh dari inti, sehingga lebih mudah “lepas” saat bereaksi. Fenomena alam ini membuktikan bahwa tabel periodik sebenarnya adalah peta kekuatan energi atom, bukan sekadar daftar nama. Dengan memahami prinsip ini, Anda sudah menguasai karakteristik seluruh golongan tanpa menghafal satu per satu.
Logika Elektron Valensi dalam Kehidupan Sehari-hari
Rahasia utama dalam cara memahami tabel periodik kimia terletak pada angka golongan yang menunjukkan jumlah elektron valensi. Anggap saja elektron valensi sebagai “tangan” yang digunakan atom untuk berpegangan dengan atom lain.
-
Golongan 1 (Alkali): Hanya punya satu tangan, sehingga sangat agresif mencari pasangan.
-
Golongan 18 (Gas Mulia): Sudah punya delapan tangan yang saling mengunci (stabil), sehingga mereka cenderung “sombong” dan tidak mau bereaksi dengan unsur lain.
Kita bisa melihat contoh nyata pada garam dapur (NaCl). Natrium yang punya satu elektron berlebih memberikannya kepada Klorin yang kekurangan satu elektron. Hasilnya? Sebuah ikatan yang sangat stabil. Memahami interaksi ini jauh lebih bermanfaat daripada sekadar menghafal nomor atom, karena Anda mulai melihat bagaimana dunia ini terbentuk dari transaksi elektron.
Periodisitas dan Tren Sifat Unsur yang Konsisten
Selain kolom vertikal (golongan), baris horizontal atau periode juga menyimpan cerita yang logis. Saat Anda bergerak dari kiri ke kanan dalam satu periode, sifat unsur berubah secara bertahap dari logam yang sangat reaktif menjadi non-logam, dan berakhir pada gas mulia.
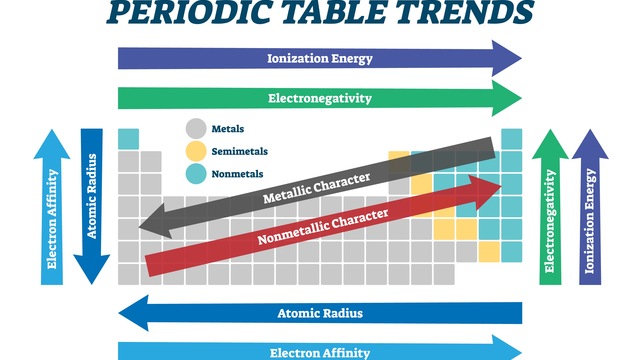
Hal ini terjadi karena jumlah proton di inti atom bertambah, yang kemudian menarik elektron lebih kuat ke arah pusat. Akibatnya, atom di sisi kanan tabel cenderung lebih “pelit” membagikan elektronnya (elektronegativitas tinggi). Dengan memahami tren jari-jari atom dan elektronegativitas ini, Anda bisa menebak mana unsur yang kuat menarik elektron dan mana yang mudah melepasnya hanya dengan melihat posisinya.
Mengamati Fenomena Reaktivitas di Laboratorium Sekolah
Untuk benar-benar meresapi ilmu ini, kita harus sering melakukan observasi pada fenomena nyata. Misalnya, mengapa tembaga (Cu) digunakan untuk kabel listrik sedangkan oksigen (O) justru menjadi gas yang kita hirup? Hal ini berkaitan dengan posisi mereka di tabel periodik yang menentukan kemampuan menghantarkan arus.
Eksperimen sederhana seperti pembakaran pita Magnesium (Mg) menunjukkan betapa teraturnya alam ini. Magnesium berada di Golongan 2 (Alkali Tanah), yang reaktif namun tidak se-ekstrem Golongan 1. Keindahan cara memahami tabel periodik kimia adalah saat Anda menyadari bahwa setiap ledakan, perubahan warna, dan pembentukan kristal di laboratorium hanyalah manifestasi dari angka-angka di tabel tersebut yang sedang “beraksi”.